 Полная версия
Полная версияПолная версия:
Рекомендации ESPEN-ESPGHAN-ECFS по диетотерапии при муковисцидозе у младенцев, детей и взрослых
Рекомендации: селен
Пищевые добавки с селеном:
Мы не рекомендуем рутинное применение пищевых добавок с селеном у больных с MB (уровень доказательности: низкий).
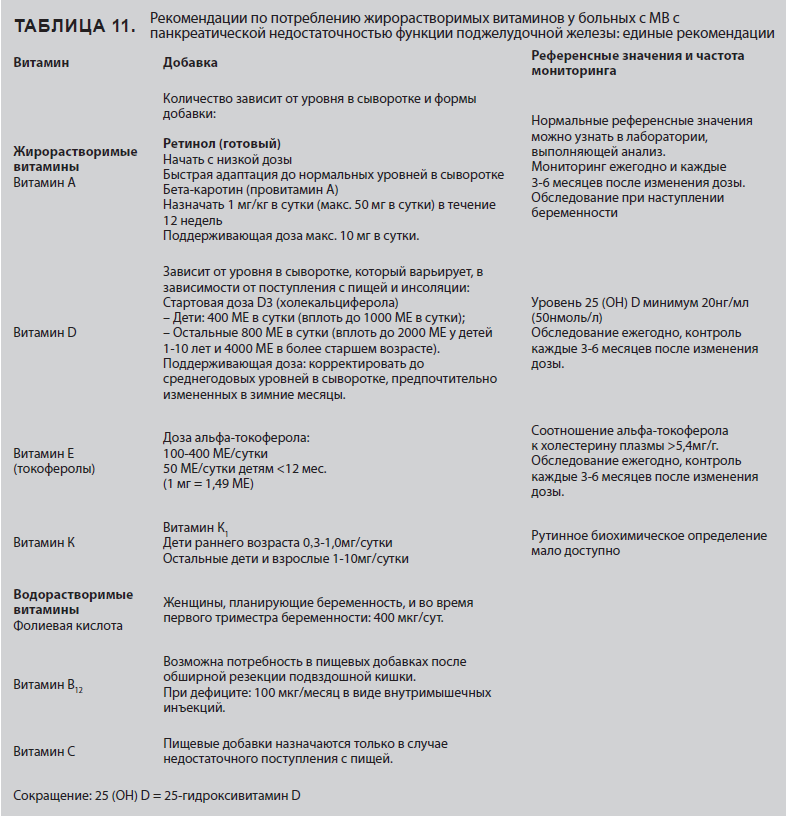
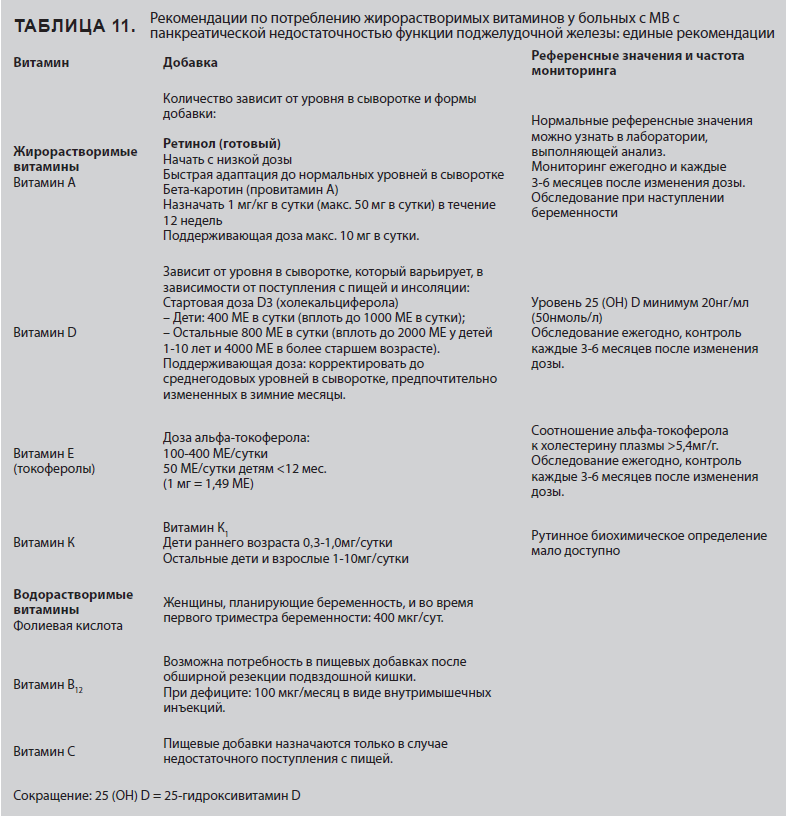
3.5 Жирорастворимые витамины (Таблица 11)
Нарушение механизма всасывания жиров, обусловленное недостаточностью поджелудочной железы, может вызвать у больных с MB дефицит жирорастворимых витаминов, в частности витаминов А, Е и К. Без адекватной инсоляции у этих пациентов также может развиться дефицит витамина D[308]. Обнаружено, что даже при сохранной функции поджелудочной железы у пациентов с MB может иметься риск развития дефицита жирорастворимых витаминов[309].
Дефицит жирорастворимых витаминов встречается часто, возникая у 10–35 % детей с панкреатической недостаточностью [ПО]. Однако у пациентов с MB явные клинические признаки дефицита, как правило, отсутствуют. Поэтому целью обследования и лечения является коррекция субоптимальных уровней и достижение оптимальных биохимических значений этих витаминов[310]. У всех пациентов с MB уровни жирорастворимых витаминов в плазме следует определять минимум один раз в год.
У больных с панкреатической недостаточностью мы рекомендуем определение уровней жирорастворимых витаминов после начала ферментотерапии и введения витаминных добавок, через 3–6 месяцев после начала или коррекции доз витаминотерапии и далее один раз в год[311]. Витаминные добавки следует принимать вместе с пищей, богатой жирами, и с ферментами для улучшения их всасывания. При обнаружении биохимического дефицита, несмотря на адекватное поступление витаминов с пищей, перед коррекцией дозы необходимо исключить низкую приверженность к лечению или плохую абсорбцию добавок. У пациентов с сохранной функцией поджелудочной железы мы рекомендуем выполнять оценку уровня витаминов в плазме крови один раз в год.
3.5.1 Витамин А
Дефицит витамина А при MB встречается часто, обнаруживаясь у 10–40 % пациентов[312][313]. Он может развиться, независимо от возраста, нутритивного статуса, наличия мекониевого илеуса, тяжести заболевания, генотипа и состояния экзокринной функции поджелудочной железы[314]. У больных с MB низкие уровни витамина А связывают с ухудшением клинического статуса, нарушением функции легких и учащением обострений легочных заболеваний[315]. Клинические симптомы дефицита возникают чрезвычайно редко.
В литературе содержатся сведения о доброкачественном повышении внутричерепного давления (псевдоопухоли мозга), одно- или двустороннем поражении лицевого нерва у ребенка раннего возраста[316], ксерофтальмии, которая может прогрессировать до сухости конъюнктив и в конечном итоге до изъязвления роговицы и слепоты[317].
Уровень витамина А в плазме может снизиться у пациентов с недостаточностью функции поджелудочной железы, получающих заместительную ферментотерапию, а также у больных с сохраненной функцией поджелудочной железы[318]. Этот дефицит может быть последствием нарушения мобилизации печеночных запасов из-за снижения уровня ретинол-связывающего белка[319],что может возникнуть у детей с тяжелым поражением печени, гипотрофией или дефицитом цинка[320]. При тяжелом поражении печени и снижении уровня ретинол-связывающего белка количество пищевых добавок с витамином А должно быть ограниченным из-за возможности развития тяжелого гипервитаминоза[321].
Мы рекомендуем применение пищевых добавок с витамином А для достижения нормальных концентраций ретинола в сыворотке, характерных для здоровых людей; нормальный диапазон определяется в соответствии с данными лаборатории, в которой проводятся анализы[322]. При использовании ретинола начинают с низких доз, которые затем повышают, согласно рекомендациям, в зависимости от уровня в сыворотке. Бета-каротин является предшественником витамина А и, в отличие от готового ретинола, регулируется по механизму отрицательной обратной связи[323][324], и поэтому может быть более безопасным для применения[325]. Показано, что доза провитамина бета-каротина, равная 1 мг/кг массы в сутки в течение 12 недель с последующей поддерживающей дозой (максимум 10 мг в сутки) является эффективной и безопасной для детей 12–18 лет[326].
Мы рекомендуем мониторирование сывороточного уровня витамина А для контроля начальной и последующих доз витаминома А. Уровни витамина А в сыворотке не точно коррелируют с содержанием витамина А в тканях. Их не следует оценивать в острую фазу инфекций, когда концентрации ретинола в сыворотке снижаются в ответ на воспаление[327].
Высокие концентрации ретинола в сыворотке указывают на риск токсического действия, что может привести к развитию фиброза печени, снижению минерализации костной ткани и повышению риска переломов[328]. В исследованиях было продемонстрировано, что у большинства пациентов с MB, находящихся в стабильном состоянии, был превышен рекомендуемый верхний предел потребления витамина А из пищевых добавок и продуктов питания. Введение пищевых добавок не было необходимым в 20–25 % случаев[329][330].
Потенциально токсическое действие витамина А представляет серьезную проблему. При определении дозировки витамина А необходимо учитывать его токсическое действие[331]. Риск гипервитаминоза возрастает при использовании водорастворимых форм препаратов, в отличие от препаратов на жировой основе[332].
Адекватное поступление витамина А имеет большое значение перед наступлением беременности и во время нее, однако особое внимание следует уделить назначению адекватной дозы, поскольку, как гипер-, так и гиповитаминоз могут оказать вредное действие на организм как матери так и ребенка[333][334]. Мы рекомендуем оценку потребления витамина А и определение его уровня в крови до зачатия и в ранний период беременности, с поддержанием его потребления на уровне не выше 10000 ME в сутки. При низком уровне следует учесть, как пользу, так и риски дополнительного введения витамина А с пищей, как для матери, так и для ребенка.
Рекомендации: витамин А
Пищевые добавки с витамином А:
• Мы рекомендуем назначение пищевых добавок витамина А до достижения нормальных концентраций ретинола в сыворотке у здоровых лиц этого же возраста.
• Мы рекомендуем оценку потребления витамина А и его уровня в крови у женщин перед зачатием и в ранний период беременности. Мы считаем необходимым учитывать пользу и риски применения добавок витамина А, как для матери, так и для ребенка, при низких уровнях витамина А в плазме, и считаем необходимым поступление витамина А на уровне менее 1000 МЕ/сутки.
Монторинг:
• Мы рекомендуем ежегодное исследование уровня витамина А в сыворотке крови и каждые 3–6 месяцев после изменения дозы или наступления беременности (уровень доказательности: низкий).
3.5.2 Витамин D
Витамин D играет важную роль в абсорбции кальция в кишечнике и дефицит этого витамина является одним из нескольких факторов, которые способствуют снижению минеральной плотности костной ткани у больных с MB[335]. Дефицит витамина D встречается достаточно часто. Он обнаруживается у 22 % младенцев с MB во время скрининга[336]. Более чем у 90 % детей старшего возраста и взрослых с MB уровень 25-гидроксивитамина D (25(OH)D) был снижен[337].
Основной источник витамина D – инсоляция – может резко различаться у разных людей в зависимости от географической широты[338]. Лучшим показателем статуса витамина D является уровень 25(OH)D в сыворотке крови[339].
Единое мнение относительно оптимальной концентрации витамина D в сыворотке отсутствует. В выполненном недавно обзоре было обнаружено повышение уровня 25(OH)D у пациентов с MB, дополнительно получающих витамин D в виде пищевых добавок, однако доказательств пользы или вреда от этого получено не было. Специалисты Фонда муковисцидоза США рекомендуют достижение уровней витамина D более 30 нг/мл (75 нмоль/л), поскольку такой уровень обеспечивает дополнительную пользу для здоровья костей[340]. Согласно рекомендациям Европейского руководства по минерализации костной ткани при муковисцидозе, минимальный уровень 25(OH)D должен составлять 20 нг/мл (50 нмоль/л)[341].
Мы рекомендуем вводить дополнительно витамин D у больных с MB для поддержания уровня 25 (ОН) D более 20 нг/мл (50 нмоль/л)[342][343][344]. При расчете дозы следует учитывать потребление витамина D с пищей и уровень инсоляции у каждого пациента[345]. Беременным женщинам мы рекомендуем дополнительный прием витамина D в дозе 600 ME (15 мкг) в сутки[346]. Наши рекомендации согласуются с Европейскими рекомендациями относительно допустимых пределов витамина D и с рекомендациями других руководств по муковисцидозу[347][348]. Несмотря на некоторые разногласия, применение витамина D3 у больных с MB является более предпочтительным, по сравнению с витамином D2[349][350]. Мы рекомендуем контролировать уровень 25(OH)D в сыворотке крови ежегодно [25], предпочтительно в конце темного времени года, а также каждые 3–6 месяцев после изменения дозы препарата[351].
Рекомендации: витамин D
Пищевые добавки с витамином D
• Мы рекомендуем дополнительное введение витамина D для поддержания концентрации 25-гидроксивитамина D (25(OH)D) более 20 нг/мл (50 нмоль/мл).
• Мы рекомендуем безопасный уровень инсоляции.
• Беременным женщинам мы рекомендуем дополнительный прием витамина D в дозе 600 ME (15 мкг) в сутки
Мониторинг:
• Мы рекомендуем контролировать уровень 25(OH)D в сыворотке крови ежегодно, предпочтительно в конце темного времени года, а также каждые 3–6 месяцев после изменения дозы препарата.
(Уровень доказательности: низкий)
В настоящее время продолжаются споры относительно оптимального режима дозирования и наиболее эффективной формы витамина D[352]. В проведенном недавно исследовании рассматривался альтернативный способ дозирования витамина D. Shepherd с соавторами обнаружили, что однократный прием высокой дозы холекальциферола (витамина D3) внутрь, известный как метод лечения ударными дозами ("Stosstherapie") с последующей поддерживающей терапией приводил к безопасному повышению 25(OH)D и его сохранению на высоком уровне более 75 нмоль/л в течение 12 месяцев у детей с MB[353].
В выполненном недавно обзоре было обнаружено наличие сниженных уровней витамина D у многих пациентов с MB, несмотря на его дополнительный прием. Авторы предположили нарушение у этих больных биодоступности витамина D, механизм которого выходит за рамки современного представления о нарушении переваривания и всасывания жира. Авторы полагают, что статус витамина D может оказывать влияние на силу дыхательной мускулатуры, структуру и функцию легких, способность сопротивляться инфекциям и секрецию инсулина[354].
3.5.3 Витамин Е
Альфа-токоферол (а-токоферол), главное составляющее вещество витамина Е, является основным утилизатором свободных радикалов кислорода и, таким образом, помогает защитить жирные кислоты от окислительного повреждения и сохранить целостность клеточных мембран. Клинически дефицит витамина Е может привести к серьезным последствиям, таким как гемолитическая анемия, нейромышечная дегенерация, заболевания сетчатки и когнитивные расстройства. Дефицит витамина Е на биохимическом уровне встречается примерно у 23 % детей раннего возраста с только что выявленным MB[355][356] и у 14 % детей старшего возраста [ПО]. Это делает липиды плазмы крови у таких больных восприимчивыми к окислительному повреждению [11]. Индивидуальные потребности в витамине Е повышаются по мере усиления окислительного стресса во время обострения легочных заболеваний или с возрастом[357]. Хронические респираторные и воспалительные заболевания способствуют усилению окислительного стресса, что дополнительно подавляет функцию гена CFTR[358], делая еще более важным адекватное поступление витамина Е с пищей.
В четырех исследованиях, посвященных применению пищевых добавок с витамином Е у больных с MB, обнаружено, что дополнительное введение витамина Е с пищей может повысить уровень витамина Е в сыворотке крови, однако прямые доказательства благоприятного воздействия на организм пищевых добавок с витамином Е отсутствуют[359]. Необходимо также изучение пользы и рисков долгосрочного воздействия высокого уровня витамина Е в сыворотке в данной популяции больных[360]. Мы рекомендуем регулярное дополнительное введение витамина Е (а-токоферола) с пищей пациентами с MB для поддержания уровня а-токоферола в сыворотке в нормальном диапазоне. В связи с тем, что желчные кислоты необходимы для абсорбции витамина Е, больным с холестазом необходимо применение водорастворимых препаратов[361].
Традиционно уровень витамина Е в сыворотке менее 300 мкг/дл указывает на его дефицит[362]. В связи с тем, что уровень витамина Е соответствует уровню липидов, отношение а-токоферола к общему уровню липидов было предложено в качестве показателя истинного статуса витамина Е. Этот подход позволяет преодолеть влияние некоторых физиологических состояний, на фоне которых уровень витамина Е может снижаться или повышаться. Уровень витамина Е может показаться сниженным на фоне гиполипидемии. С другой стороны, уровень витамина Е может показаться высоким у некоторых больных с MB в связи с увеличением продолжительности жизни при этом заболевании и повышением уровня некоторых липидов у больных с MB пожилого возраста[363]. В таких ситуациях более точным будет показатель отношения а-токоферола к общему уровню липидов (натощак) или отношения а-токоферола к холестерину или отношения а-токоферола к полиненасыщенным жирным кислотам (не натощак). Тогда как нижней границей отношения а-токоферола к холестерину у здоровых людей считается уровень 2,47 мг/г, у пациентов с MB этот показатель рекомендуется повысить до уровня 5,4 мг/г[364]. Мы рекомендуем оценку уровня витамина Е минимум один раз в год у всех больных с MB и каждые 3–6 месяцев после коррекции дозы[365]. Между тем продолжаются споры относительно того, какой из показателей использовать в качестве биомаркера уровня витамина Е в крови: уровень а-токоферола в плазме/сыворотке или отношение а-токоферола к холестерину.
Рекомендации: витамин Е
Пищевые добавки с витамином Е:
• Мы рекомендуем регулярное применение пищевых добавок с витамином Е для поддержания отношения а-токоферола к холестерину на уровне 5,4 мг/кг
Мониторинг:
• Мы рекомендуем оценку уровня витамина Е минимум один раз в год у всех больных с MB и каждые 3–6 месяцев после коррекции дозы.
(Уровень доказательности: низкий).
3.5.4 Витамин К
У больных с MB отмечается, как правило, пониженное содержание витамина К. Его дефицит наблюдается у всех больных с клиническими проявлениями MB[366][367]. Витамин К играет важную роль в свертывании крови и формировании костей[368]; его дефицит может привести к развитию клинически значимых кровотечений (например, внутричерепных кровотечений у детей раннего возраста) и низкой минерализации костной ткани[369][370]. Наличие дефицита витамина К связывают с мальабсорбцией, длительным применением антибиотиков и поражением печени[371]. Все дети раннего возраста с MB, находящиеся на грудном вскармливании (как и здоровые дети), должны дополнительно получать витамин К с питанием.
В настоящее время отсутствуют стандартные биохимические показатели, характеризующие обмен витамина К. Его можно оценить на основании концентрации в сыворотке витамина К, PIVKA-II (белков, индуцируемых отсутствием витамина К) и некарбоксилированного остеокальцина, однако эти маркеры, как правило, не используются в повседневной клинической практике из-за высокой стоимости их анализа. Можно измерять протромбиновое время, однако этот показатель является мало чувствительным и повышается только при очень тяжелом дефиците витамина К[372].
Витамин K1 (фитоменадион, филлохинон), форма витамина К, присутствующая в зеленолистных овощах и овощном масле, рекомендуется в качестве наиболее безопасной формы пищевых добавок витамина К, более предпочтительной, по сравнению с солями менадиона. В небольшом, но тщательно проведенном исследовании было обнаружено, что ежедневное применение витамина К: в дозе 50 мг приводит к повышению уровня витамина К: в сыворотке крови у детей с MB[373].
В настоящее время недостаточно данных для определения наиболее эффективной дозы витамин K1. На сегодняшний день мы рекомендуем регулярное дополнительное введение витамина К: детям раннего возраста в дозе 0,3–1,0 мг в сутки. Для детей старшего возраста и взрослых мы рекомендуем 1-10 мг в сутки витамина К в зависимости от возраста (Таблица 11)[374]. Более высокие дозы можно рекомендовать пациентам с низким уровнем витамина К или с повышенным риском его дефицита, например, на фоне длительного приема антибиотиков[375]. Предпочтительным является ежедневный прием витамина из-за низкой его способности к накоплению[376][377].
Особое внимание следует уделять новорожденным с MB и больным с MB, получающим антибиотики широкого спектра действия, а также пациентам с поражением печени и тяжелой мальабсорбцией. Токсического действия витамина К (филлохинона) зарегистрировано не было[378].
Рекомендации: витамин К1
Пищевые добавки с витамином К:
• Мы рекомендуем регулярное применение пищевых добавок с витамином К в дозах, зависящих от возраста и группы риска: у детей раннего возраста 0,3–1 мг в стуки, у детей старшего возраста и взрослых 1-10 мг в сутки (уровень доказательности: низкий).
3.6 Водорастворимые витамины (Таблица 11)
Дефицит водорастворимых витаминов (фолиевой кислоты, витамина В12 и витамина С) при неосложненном MB встречается редко. Тем не менее, всем женщинам, планирующим беременность, мы рекомендуем дополнительное употребление 400 мг фолиевой кислоты в период, предшествующий зачатию, и в первый триместр беременности для профилактики развития дефектов нервной трубки [16]. Дефицит витамина В12 может возникнуть у пациентов, которым была выполнена обширная резекция терминального отдела подвздошной кишки в связи с осложненным мекониевым илеусом. Некоторым из этих больных может потребоваться пожизненное применение витамина В12 в дозе 100 мкг в месяц, который будет вводиться парентерально. Дополнительное введение витамина С может потребоваться лицам с риском развития его дефицита из-за низкого поступления с пищей (особенно с овощами и фруктами). В этих случаях следует ориентироваться на рекомендации, прописанных в руководствах, и в случае дефицита применять пищевые добавки с витамином С.
Рекомендации: фолиевая кислота
• Женщинам, планирующим беременность, мы рекомендуем дополнительное употребление 400 мг фолиевой кислоты в период, предшествующий зачатию, и в первый триместр беременности (уровень доказательности: низкий).
3.7 Лечение панкреатической недостаточности
Заместительная терапия панкреатическими ферментами (ЗТПФ, PERT) является жизненно необходимой для поддержания адекватного статуса питания. Эффективность этого метода лечения была доказана[379][380]. ЗТПФ предполагает прием внутрь ферментов поджелудочной железы, особенно протеазы и липазы с целью введения ферментов в просвет двенадцатиперстной кишки для переваривания белков и жиров, попадающих туда из желудка[381].
Панкреатические ферменты, как правило, назначаются внутрь в виде таблеток, покрытых кишечно-растворимой оболочкой, или в виде микросфер, что предотвращает их инактивацию кислотой желудочного сока и обеспечивает их доставку в двенадцатиперстную кишку[382]. Микросферы, покрытые кишечно-растворимой оболочкой, возможно, являются более эффективными, чем таблетки, покрытые кишечно-растворимой оболочкой. Эффективность ЗТПФ может быть повышена на фоне применения ингибиторов протонной помпы. Рекомендуемые нами дозы согласуются с дозами, рекомендуемыми Руководством Североамериканского фонда муковисцидоза по потреблению липазы, в зависимости от возраста, массы тела и количества потребляемых жиров (Таблица 12). Для детей раннего возраста эти дозы также соответствуют рекомендациям другого недавно выпущенного руководства.
В клинической практике назначение ферментов в виде микросфер детям раннего возраста представляет определенные трудности. Если ребенок отказывается принимать микросферы с водой или молоком, можно попробовать дать его с яблочным пюре. Если и так ребенок отказывается от приема микросфер, временно можно применять незащищенные ферменты. Панкреатические ферменты не следует никогда добавлять в питание. У пациентов всех возрастов ферменты в виде порошков можно использовать, для улучшения полостного пищеварения, когда, например, назначение ферментов внутрь невозможно, или когда требуется питание через еюностому Ферменты, назначаемые в такой ситуации, не следует назначать с питанием. Их следует вводить болюсно через трубку для энтерального питания. При использовании незащищенных ферментов одновременное применение ингибиторов протонной помпы может помочь предотвратить разрушение липазы желудочным соком. У детей раннего возраста была доказана безопасность препаратов панкреалипазы, покрытых кишечно-растворимой оболочкой. Родители предпочитают использовать именно эти препараты[383][384][385][386][387][388].
В настоящее время отсутствуют данные о наиболее оптимальном времени начала лечения или метода коррекции доз ферментов у больных с панкреатической недостаточностью разной степени тяжести. Для получения ответа на эти вопросы необходимо проведение тщательно разработанных исследований.
Пациентам, получающим ЗТПФ, мы рекомендуем регулярный контроль роста и/или нутритивного статуса для оценки адекватности лечения [136] – при каждом посещении врача для детей раннего возраста, каждые 3 месяца для детей старшего возраста и подростков и каждые 6 месяцев для взрослых.
Рекомендации: заместительная терапия ферментами поджелудочной железы
• Мы рекомендуем заместительную терапию ферментами поджелудочной железы (ЗТПФ) всем пациентам с панкреатической недостаточностью.
• Мы рекомендуем контроль роста и/или нутритивного статуса для оценки адекватности лечения: при каждом посещении врача для детей раннего возраста, каждые 3 месяца для детей старшего возраста и подростков и каждые 6 месяцев для взрослых, (уровень доказательности: низкий)

4. Питание истощенных пациентов с МВ
Недостаточное питание, как описано в Таблице 13, остается проблемой многих пациентов с MB. несмотря на постоянный прогресс в лечении дыхательных расстройств и диетотерапии в последние несколько десятилетий. За пациентами с MB необходимо регулярно наблюдать и оценивать их рост и нутритивный статус (см. Оценку нутритивного статуса), чтобы на ранней стадии выявлять нарушения и лечить их. Ухудшение роста, несмотря на правильную ЗТПФ и лечение проблем легких, можно объяснить нехваткой общего количества энергии и дефицитом НЖК[137][138][139]. Нутритивная поддержка должна быть обусловлена индивидуальными потребностями пациента с учетом возраста, нутритивного и панкреатического статусов, домашних условий, пищевых особенностей, связанных с религиозными и культурными представлениями, и предпочтениями в еде.
Как отмечается в Кокрановских обзорах, контролируемые исследования, оценивающие эффективность диетотерапии при недостаточности питания у пациентов с MB, имеют ряд недостатков и ограничений[140]. В отсутствие таких данных, современные директивы по питанию из Европы, Великобритании и США, а также настоящее руководство содержат рекомендации по профилактике нехватки питательных веществ, сформулированные главным образом на основе заключения экспертов.
4.1 Прогрессирование болезни и усиленное питание
Раньше рекомендации по питанию выносились с учетом веса, роста и массо-ростового индекса (МРИ) в качестве основного параметра для принятия решения о том, когда требуется начать интенсивную нутритивную терапию. В последнее время Stallingsetal. рекомендуют использовать перцентили ИМТ (для детей) и значения ИМТ (для взрослых) как более точный показатель нутритивного риска. В настоящих рекомендациях для принятия решений будет применяться этот подход (Таблица 13). Другими причинами для проведения профилактической нутритивной терапии являются риск энергетического дисбаланса, наличие рецидивирующих легочных инфекций или вступление в период активного роста.



