
Полная версия:
Артериальная гипертензия. Путь к здоровью сосудов и сердца
Водно-электролитный баланс. Глюкокортикоиды аналогично альдостерону (минералокортикоиду) повышают реабсорбцию (задерживают) ионов натрия и, соответственно, воды. При этом также происходит увеличение выведения ионов калия и магния. Однако данное действие выражено в меньшей степени по сравнению с эффектом альдостерона. Также глюкокортикоиды, в отличие от альдостерона оказывают влияние на обмен кальция:
· уменьшают всасывание ионов кальция в желудочно-кишечном тракте;
· повышают экскрецию ионов кальция почками;
· снижают включение ионов кальция в костную ткань.
Таким образом, длительное высвобождение глюкокортикоидов вызывает значительные сдвиги гомеостаза внутренней среды организма, что проявляется, в частности, значительными изменениями со стороны центральной нервной системы и сердечно-сосудистой системы.
Выявлено, что глюкокортикоиды оказывают стимулирующее действие на центральную нервную систему (ЦНС), что вызывает такие изменения как бессонница, повышенная возбудимость, нарушение поведения и т. д.
Влияние глюкоортикоидов на сердечно-сосудистую систему проявляется в:
· повышении тонуса сосудов (спазм) и сократимости (сила сокращений) миокарда, что связано с:
– активацией ЦНС,
– увеличением чувствительности адренорецепторов к медиаторам – норадреналину и адреналину,
– увеличением чувствительности рецепторов ангиотензина к медиатору – ангиотензина II;
· увеличением объема циркулирующей крови (ОЦК) из-за повышения реабсорбции ионов натрия и воды и т. д.
В заключение раздела хотим еще раз обратить ваше внимание на следующий факт. Все перечисленные механизмы стимуляции деятельности сердечно-сосудистой системы направлены на преодоление стрессовых ситуаций: догнать, обогнать, не допустить смерти при кровопотери. То есть реализация их действия кратковременна – часы, дни. В этом случае все описанные изменения носят компенсаторный характер. Длительная активация приводит к развитию различных патологических состояний, в том числе и гипертонической болезни, о механизме развития которой вы сможете прочитать ниже.
Эндотелины
Группа соединений, обладающих высокой биологической активностью – эндотелины, впервые была выделена из эндотелиальных клеток сосудов. Известно четыре типа эндотелинов (ЭТ) – ЭТ1, ЭТ2, ЭТ3, и ЭТ4. По химической природе они являются пептидами, содержат 21 остаток аминокислот и отличаются друг от друга аминокислотной последовательностью. Основным и общим эффектом эндотелинов является повышение тонуса сосудов и, как следствие, артериального давления. Среди этой группы соединений наиболее изучен ЭТ1.
Эндотелин-1 является одним из самых мощных вазоконстрикторов. Его синтез осуществляется в эндотелиальных клетках сосудов и включает несколько стадий. Из предшественника эндотелинов (препроэндотелина) образуется «большой эндотелин» (проэндотелин), который, в свою очередь, под действием эндотелин-превращающего фермента (ЭПФ) трансформируется в активный полипептид, состоящий из 21 аминокислоты – эндотелин-1.
Образование ЭТ1 в эндотелиальных клетках повышается под влиянием таких соединений и факторов как:
· катехоламины,
· ангиотензин II,
· тромбин,
· антидиуретический гормон (вазопрессин),
· интерлейкин-1,
· свободные радикалы – активные формы кислорода,
· гипоксия,
· повышение артериального давления,
· ускорение кровотока и т. п.
Концентрация ЭТ1 в крови повышается при патологии сердечно-сосудистой системы и является возможным маркером повреждения клеток эндотелия и/или миокарда, в большей степени, чем причиной легочной гипертензии в малом круге кровообращения.
В результате взаимодействия ЭТ1 со специфическими эндотелиновыми рецепторами, расположенными на наружных клеточных мембранах (ЭТА и ЭТВ), повышается внутриклеточная концентрация ионов кальция. С рецепторами ЭТА взаимодействует (селективно) только ЭТ1, а с рецепторами ЭТВ – все три типа эндотелинов.
В физиологических условиях концентрация ЭТ1 в плазме очень низкая, что связано, прежде всего, с ингибированием (торможением) синтеза эндотелина-1 соединениями, вызывающими вазодилатацию (оксидом азота и простациклином). В этих физиологических количествах ЭТ1 активирует образование эндотелиальными клетками данных факторов релаксации. В высоких концентрациях ЭТ1, стимулируя рецепторы ЭТА и ЭТВ гладкомышечных клеток, вызывает стойкое и выраженное сужение сосудов.
Основные эффекты стимуляции специфических эндотелиновых рецепторов эндотелином-1 представлены в таблице 4.

Таблица 4. Основные эффекты стимуляции специфических эндотелиновых рецепторов эндотелином-1
Взаимодействие всех изоформ ЭТ с ЭТВ-рецепторами приводит как к вазоконстрикции, так и вазодилатации за счет стимуляции синтеза NO-радикала и простациклина. Однако вазоконстрикция, вызванная активацией ЭТА-рецепторов выражена в большей степени, а роль рецепторов ЭТВ в регуляции сосудистого тонуса еще недостаточно изучена.
Другие эффекты ЭТ1:
· повышение периферических и центральных эффектов активации симпатической нервной системы;
· антидиуретическое действие;
· стимуляция синтеза и секреции ренина, ангиотензина II, альдостерона и адреналина;
· в пороговых и субпорговых концентрациях усиливает контрактильный (сократительный) ответ миокарда и сосудов на другие вазоконстрикторы – норадреналин и серотонин;
· митогенный эффект;
· стимуляция апоптоза (программированная смерть клеток).
Эндотелин-2 (ЭТ2) – подтип, который отличается от эндотелина-1 двумя аминокислотными остатками в структуре N-концевого участка.
Основные эффекты эндотелина-2:
· обладает положительным хронотропным действием, провоцируя развитие аритмий;
· участвует в патофизиологических процессах при сердечной недостаточности;
· снижает толерантность к физическим нагрузкам при сердечно-сосудистой патологии;
· потенцирует лёгочную гипертензию;
· ухудшается течение диабетической кардиомиопатии при повышения содержания ЭТ2 в сердце;
· способствует ремиелинезации клеток центральной нервной системы;
· нарушается процесс овуляции при недостатке ЭТ2;
· оказывает влияние на процессы терморегуляции, иммунологические реакции и некоторые другие процессы.
Эндотелин-3 (ЭТ3) – это пептид, включающий 21 аминокислотный остаток, образуется из предшественника и взаимодействует с рецептором ЭТВ. Является одним из регуляторов функционального состояния эндотелия сосудов. В значительных количествах определяется в головном мозге, кишечнике, почках и легких.
Основные эффекты эндотелина-3:
· играет роль в поддержании водно-солевого баланса;
· снижает выраженность воспалительных реакций (в низких концентрациях);
· участвует в регуляции пролиферации эпителиальных клеток (особенно бокаловидных) и повышает их устойчивость к неблагоприятным воздействиям;
· подавляет рост раковых клеток;
· оказывает влияние на формирование энтеральной нервной системы – части вегетативной нервной системы, регулирующей работу гладких мышц внутренних органов;
· оказывает влияние на развитие болезни Гиршпрунга, которая характеризуется патологией развития толстой кишки и ее иннервации.
При артериальной гипертензии эндотелин-3 вызывает сужение сосудов в легких за счет стимуляции рецепторов эндотелина типа В при низкой концентрации, а при большой – рецепторов эндотелина типа А.
Эндотелин-4 (ЭТ4) – в основном обнаружиается в кишечнике, где подобно эндотелину-1, стимулирует лейкоциты после, например, ишемии кишечника, что приводит к дальнейшему повреждению тканей. Аналогичный эффект наблюдается в легких и других органах. Также эндотелин-4 повышает выработку моноцитами альфа-фактора некроза опухоли, интерлейкина-8 и гранулоцитарно-макрофагального колониестимулирующего фактора.
Различные факторы, участвующие в регуляции артериального давления
Помимо основных и наиболее изученных механизмов, оказывающих влияние на артериальное давление, в организме существует еще ряд систем и составляющих уже представленных систем, участвующих в регуляции этого показателя.
Ангиотензин (1—7). Как было представлено на схеме 7 в различных органах и тканях из ангиотензина I при участии фермента эндопептидазы синтезируется ангиотензин (1—7). Синтез АТ- (1—7) повышается при угнетении образования ангиотензина II и накоплении АТ-I в крови и тканях, в частности, при применении ингибиторов АПФ. Предполагается, что в патогенезе различных патологических состояний сердечно-сосудистой системы играет роль не только гиперпродукция ангиотензина II, но и уменьшение синтеза и/или активности ангиотензина (1—7), который обеспечивает обратную связь и играет важную роль в регуляции прессорного (сосудосуживающего) эффекта ангиотензина II.
Физиологическая роль ангиотензина (1—7):
· вазодилататор – сосудорасширяющий эффект;
· антипролиферативное действие;
· стимуляция образования клетками эндотелия NO-радикала и некоторых простагландинов;
· повышение выведения ионов натрия и воды почками.
Таким образом, ангиотензин (1—7) является антагонистом ангиотензина II, что поддерживает определенное равновесие между разнонаправленными эффектами соединений на тонус гладких мышц сосудов, пролиферацию (размножение, деление) клеток, выведения ионов натрия и воды почками и другие.
Калликреин-кининовая система. Калликреины по химической структуре являются пептидами и широко представлены в организме млекопитающих и человека. В наибольшем количестве они определяются в тканях с экзокринной функцией (поджелудочная железа и другие) и их секретах (панкреатический сок и т.д.), в эндотелии сосудов, сердце (кардиомиоцитах), в центральной нервной системе и периферических нервных волокнах.
Калликреин-кининовая система обладает широким спектром регулирующих функций, участвуя в регуляции таких физиологических показателей как артериальное давление, функциональное состояние почек, а также в процессах адаптации, роста и размножения клеток и т. д. По мнению ряда авторов, кинины осуществляют функциональную связь между тонусом сосудистой стенки и реологическими (система свертывания крови и антисвертывающая система) свойствами крови, что особенно важно при развитии патологии со стороны сердечно-сосудистой системы.
Наиболее изученным соединением из этой достаточно большой группы веществ является брадикинин – пептид, состоящий из 9 аминокислотных остатков. Он образуется из кининогенов. Высокомолекулярный кининоген синтезируется в печени, а низкомолекулярный кининоген – непосредственно в клетках различных органов и тканей. Далее под влиянием ферментов они преобразуются в брадикинин (схема 8).
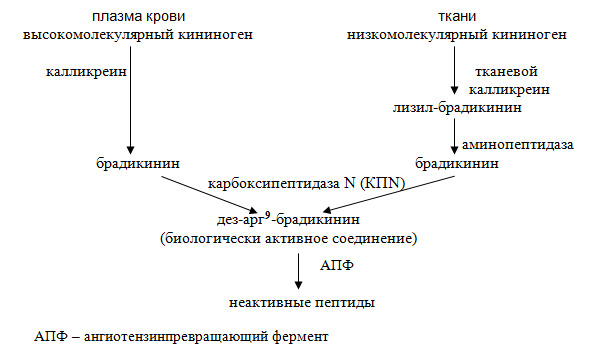
Схема 8. Синтез и деградация брадикинина
Следует обратить внимание на то, что инактивация (разрушение) брадикинина происходит при участии ангиотензинпревращающего фермента (АПФ), который катализирует реакцию образования ангиотензина II.
Среди основных эффектов брадикинина выделяют:
• выраженное сосудорасширяющее действие за счет:
– повышения высвобождения оксида азота (NO-радикал),
– стимуляции специфических (брадикининовых) В2-рецепторов,
– стимуляции синтеза и/или секреции:
а) эндотелийзависимого фактора релаксации,
б) простациклина;
• кардиопротективное действие.
Также брадикинин оказывает влияние на процесс свертывания крови:
• играет важную роль в поддержании фибринолитической активности;
• оказывает антиагрегантное действие за счет стимуляции продукции:
– оксида азота,
– простациклина,
– тканевого активатора плазминогена.
Таким образом, активация калликреин-кининовой системы в целом приводит к снижению артериального давления, повышению активности противосвертывающей системы крови и другим эффектам, противостоящим действию симпатической нервной системы и ренин-ангиотензин-альдостероновой системы.
Роль брадикининовой системы при патологии сердечно-сосудистой системы изучена недостаточно, но есть доказательства, что положительные эффекты применения ингибиторов АПФ (см. ниже) на ремоделирование сосудов и сердца могут быть связаны с увеличением концентрации брадикинина в крови.
Оксид азота (NO-радикал) – синтез NO-радикал из L-аргинина в клетках млекопитающих катализируется тремя изоформами синтетазы оксида азота (NOS). Конституитивно (то есть постоянно, без дополнительных воздействий) экспрессированы изоформы I типа (nNOS, neuronal) и III типа (eNOS, endothelial). При стимуляции липополисахаридами, цитокинами и т. д. происходит индукция II типа или индуцибельной NOS (iNOS, inducible). Изоформы nNOS и eNOS являются кальцийзависимыми ферментами и участвуют в регуляции функции нервной системы и сосудов, соответственно.
Период полужизни NO-радикала – менее 5 секунд, то есть его действие может проявляться только местно там, где он синтезировался. Среди наиболее важных эффектов отмечают:
· снижение тонуса гладких мышц сосудов в результате угнетения их сократительной функции – стимуляция растворимой гуанилатциклазы и повышение синтеза циклического гуанозин-3», 5» -монофосфата (цГМФ), что и вызывает расширение сосудов;
· торможение адгезии (прилипания) тромбоцитов и лейкоцитов к клеткам эндотелия за счет блокады экспрессии специфических молекул – молекул адгезии, стимулирующих этот процесс;
· угнетение пролиферации гладкомышечных клеток;
· торможение образования эндотелина;
· увеличение натрийуреза (выведения ионов натрия) и экскреции ренина;
· снижение окисления липопротеидов низкой плотности (ЛНП).
Считается, что NO-радикал является физиологическим антагонистом ангиотензина II.
Эндотелийзависимый фактор релаксации. Многие авторы считают, что по химической структуре этот фактор является суммой эпоксигеназных метаболитов арахидоновой кислоты (ЕЕТS). Под влиянием этих соединений активируются энергонезависимые калиевые каналы, что приводит к снижению тонуса сосудов. В наибольшей степени данный фактор оказывает влияние на гладкомышечные клетки небольших артерий.
Простациклин (PGI2) образуется в основном эндотелиальными клетками. Он активирует аденилатциклазу гладкомышечных клеток сосудов, увеличивая образование циклического аденозинмонофосфата (цАМФ). Это приводит именно в этих клетках к снижению их тонуса и, соответственно, расширению сосудов Простациклин также усиливает вазодилятацию (расширение сосудов), вызываемую NO-радикалом, и обладает синергизмом с NO в отношении торможения агрегации тромбоцитов, что препятствует образованию тромбов.
Следует обратить внимание тот факт, что при многих патологичеких состояниях – гипертонической болезни, при развитии ХСН и т.д., происходит ремоделирование сосудов и нарушение функции эндотелия. На этом фоне (эндотелиальной дисфункции) нарушается как синтез и секреция (высвобождение) соединений, способствующих расширению сосудов, так и способность клеток гладкомышечного слоя воспринимать их «сигналы». Таким образом, нарушается нормальная функциональная активность стенки сосуда и заболевание прогрессирует.
Предсердный натриуретический фактор (ПНУФ). Предсердный натрийуретический фактор был открыт сравнительно недавно – в 1981 году. Описано несколько биологических активных веществ, которые объединены в единую систему, получившую название по первому соединению – система предсердного натрийуретического фактора. Считается, что система ПНУФ является основным фактором, оказывающим противоположное действие по сравнению РААС, САС и вазопрессином.
Наиболее полно охарактеризованы три основных пептида системы ПНУФ:
· предсердный натрийуретический пептид (ПНП, ANP) содержит 28 аминокислотных остатков; синтезируется в предсердиях и в значительно меньшей степени – в желудочках сердца, а также в головном мозге, передней доле гипофиза, почках и лёгких;
· мозговой натрийуретический фактор (МНФ, BNP) включает 32 аминокислотных остатка, синтезируется, в основном, в миокарде желудочков и в незначительной степени в предсердиях и головном мозге;
· натрийуретический пептид-С (ЦНП, CNP) – точное количество аминокислотных остатков не установлено, некоторые одноцепочечные пептиды состоят из 17 аминокислотных остатков; синтезируется эндотелиальными клетками сосудов, а также в незначительном количестве образуется в головном мозге, эпителиальных клетках канальцев и собирательных трубочках почек; отличительная особенность – не имеет рецепторов в почках.
В отличие от CNP предсердный натрийуретический фактор и мозговой натрийуретический фактор синтезируются в кардиомиоцитах, обладают одинаковым механизмом действия и функционируют как двойная сердечная пептидная натрийуретическая система.
Секреция ПНУФ и МНФ регулируется растяжением предсердий и повышением трансмурального предсердного давления. Циркулируя в кровеносном русле, натрийуретические пептиды реализуют свои эффекты, взаимодействуя со специфическими рецепторами и повышая содержание в клетках-мишенях циклический гуанозинмонофосфат (цГМФ). В клетках почечного эпителия, гладких мышц артерий, в коре надпочечников и гипофиза, а также в легких, печени и тонком кишечнике выявлены специфические рецепторы ПНУФ и МНФ. Период полужизни ПНУФ и МНФ состаляет около 2,5 минут. Они инактивируются при участии фермента – нейтральной эндопептидазы (НЭП) или в результате связи со специфическими рецепторами, которые ответственны за их клиренс (выведение).
Основными физиологическими эффектами предсердного натрийуретического фактора (ПНУФ) являются:
1. Влияние на функциональную активность почек направлено на увеличение выделения ионов натрия и воды (натрийурез и диурез):
• действие в области клубочков:
– релаксация приносящих сосудов почек и сужение выносящих,
– повышение клубочковой фильтрации за счет увеличения гидростатического давления;
• увеличение скорости кровотока в сосудах мозгового вещества почек;
• непосредственное влияние на почечные канальцы и собирательные трубочки (проксимальный и дистальный отделы петли Генле) – снижение реабсорбции ионов натрия и воды;
• уменьшение секреции ренина;
2. Экстраренальные эффекты:
• угнетение высвобождения вазопрессина;
• снижение секреции альдостерона, вызванной ангиотензином II и аденокортикотропным гормоном в клетках клубочковой зоны коры надпочечников;
• уменьшение образования и угнетения активности антидиуретического гормона;
• угнетение эффектов ангиотензина II – увеличение реабсорбции ионов натрия и воды, замедление клубочковой фильтрации;
• выраженное спазмолитическое действие на гладкие мышцы сосудов ярко проявляется при предварительной констрикции (сокращении) ангиотензином II, норадреналином или вазопрессином; в результате снижается систолическое артериальное давление, происходит дилатация (расширение) коронарных артерий, причем без дополнительного использования энергии, тогда как для других процессов вазодилатации необходимы определённые энергозатраты;
• вызывает дилатацию коронарных артерий без дополнительных энергозатрат;
• улучшает сократительную функцию миокарда (увеличивает сердечный выброс) не только в связи с уменьшением сопротивления периферических сосудов (уменьшение постнагрузки на миокард), но и в результате снижения преднагрузки при сохранении адекватного венозного возврата к сердцу;
• обладает прямым положительным инотропным эффектом – увеличивает силу сердечных сокращений.
Как отмечалось, по действию на органы-мишени система ПНУФ является антагонистом РААС и в норме находится в равновесии с ней. При развитии патологии сердечно-сосудистой системы, к сожалению, «запас прочности» защитных возможностей ПНУФ быстро исчерпывается и на первый план выходят эффекты РААС.
Взаимосвязь различных систем, регулирующих артериальное давление
Как уже неоднократно отмечалось, все в организме взаимосвязано. В таблице 5 представлены системы, оказывающие противоположное влияние на функциональную активность сердечно-сосудистой системы.
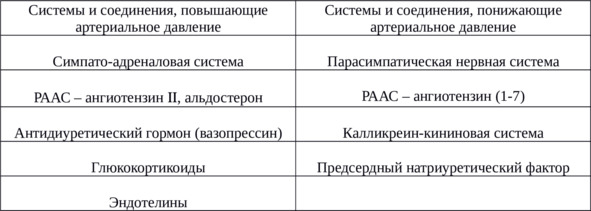
Таблица 5. Основные системы и соединения, участвующие в регуляции артериального давления
Наиболее наглядно принципы взаимосвязи различных систем, приводящих в конечном итоге к повышению артериального давления, можно продемонстрировать на примере кратковременной стрессовой реакции, будь то тяжелая физическая или психическая нагрузка. И в первом, и во втором случае «включаются» механизмы, направленные на ее выполнение. И еще раз подчеркнем. В течение миллионов лет совокупность этих процессов была направлена на поддержание гомеостаза организма в течение небольшого промежутка времени (в большинстве случаев физической нагрузки), а затем у современного человека на первый план вышли процессы, поддерживающие постоянство внутренней среды в «нормальных», неэкстремальных условиях.
Механизмы приспособления гемодинамики к физической работе представляют теоретический и практический интерес. Для осуществления дополнительной нагрузки органы и ткани организма должны получать большее, чем в состоянии покоя, количество кислорода и питательных веществ, которые переносятся кровью. При подготовке и в процессе физической деятельности импульсы поступают от скелетных мышц к головному мозгу. В этом случае в первую очередь происходит активация центральной нервной системы – стимуляция симпатики, что приводит к разнообразным изменениям (схема 9):
· повышается частоты сердечных сокращений и сердечного выброса, одновременно расширяются сосуды, кровоснабжающие скелетные мышцы, а кровоток в сосудах кожи и органах брюшной полости снижается;
· увеличивается секреция адреналина, который взаимодействует с адренорецепторами, и еще в большей степени усиливает эффекты стимуляции симпатики, а также вызывает повышение глюкозы в крови – основного соединения, необходимого для синтеза соединений, являющихся аккумуляторами энергии в клетках (АТФ, АДФ и др.);
· повышается активность циркуляторной РААС, стимулируется продукция АДГ (вазопрессина) – увеличивается объем циркулирующей крови;
· увеличивается высвобождение АКТГ, что приводит к повышению секреции глюкокортикоидов и, соответственно, глюкозы в крови и т. д.
Выше перечислены только самые значимые изменения. Однако проанализировав все, о чем упоминалось в предшествующих разделах, можно составить практически полную картину всех протекающих процессов.
После выполнения поставленных задач все параметры нормализуются и на первый план выходят эффекты стимуляции парасимпатической нервной системы, о которых сказано выше.
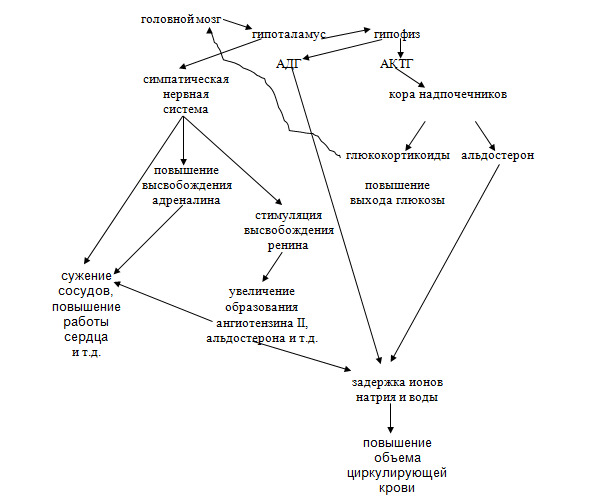
Схема 9. Взаимосвязь систем, регулирующих состояние сердечно-сосудистой системы
А что такое артериальная гипертензия?
Наверное, многим измеряли артериальное давление. При этом врач называет две цифры, например 120 на 80, которые наиболее часто записывают в виде дроби 120/80. А что они означают? Итак, при измерении артериального давления (АД) получают два показателя. Числитель дроби (большая цифра) обозначает наивысшее давление крови на стенку сосуда сразу после систолы (сокращения) сердца, так называемое систолическое («верхнее», «сердечное») давление. Цифра в знаменателе обозначает диастолическое («нижнее», «сосудистое») артериальное давление, которое характерно для диастолы (расслабления) сердца и отражает, в определенной степени, тонус сосудистой стенки. Во всем мире единицей измерения артериального давления являются миллиметры ртутного столба (мм рт. ст.). В настоящее время считается, что артериальное давление выше 140/90 является признаком гипертонии.
В норме артериальное давление непостоянно и изменяется в течение суток:
· с 1:00 до 5:00 утра давление самое низкое,
· с 6:00 до 8:00 резко повышается,
· затем в течение дня практически не меняется и

