
Полная версия:
Пособие по неорганической химии

Фаина Лубенская
Пособие по неорганической химии
Автором данного пособия является Лубенская Ф. Л., Заслуженный учитель РСФСР и Отличник народного просвещения.
Выражается благодарность инженеру-химику Шиверской И. П., принявшей активное участие в редактировании текста данного пособия.
Химия – наука чудес, в ней скрыто счастье человеческое.
М. ГорькийШироко простирает химия руки свои в дела человеческие.
(М. ЛомоносовОбщая химия
Введение
Явления физические и химические
Происходящие с телами изменения называются явлениями.
Явления, при которых состав вещества остается неизменным – это физические явления. При физических явлениях происходит изменение формы, агрегатного состояния, температуры вещества.
Пример. При нагревании воды она будет испаряться, а при температуре ниже 0°C – превращаться в лед, однако ее состав при этих превращениях не изменяется.
Явления, при которых вещество претерпевает глубокие изменения, в результате чего получается вещество с новыми свойствами, называются химическими явлениями.
Химические явления составляют основу жизни всей природы.
Химические процессы (вместе с физическими) определяют состав нашей планеты. Эти же процессы создают почву, ткани растений и животных.
Химические изменения поддерживают жизнь всех организмов. В результате химических явлений происходит превращение одних веществ в другие, т.е. изменяется состав молекул – образуются молекулы новых веществ.
Примеры химических явлений. Железо во влажном воздухе покрывается ржавчиной – образуется оксид железа (Fe2O3). Медные пластины при нагревании теряют свой блеск и покрываются налетом черного цвета: оксидом меди (CuO). Лента металлического магния горит ослепительно ярким светом, образуя порошок белого цвета – оксид магния (MgO).
Процесс превращения одних веществ в другие, отличающиеся составом и свойствами от исходных веществ – называется химической реакцией.
Химическая реакция – это процесс превращения одних веществ в другие без изменения общего числа и природы атомов, из которых эти вещества состоят.
Способ выражения химической реакции, его качественной и количественной сторон – это уравнение химической реакции, где отражены химические формулы и уравнения, описывающие состав и их химическое строение.
Пример химической реакции:
NaOH + HCl = NaCl + H2O
Уравнения химических реакций основаны на законе массы реагирующих веществ (М. В. Ломоносов). Поскольку при химических реакциях атомы сохраняются, масса атомов, вступивших в реакцию, в точности равна массе атомов, содержащихся в продуктах реакции – это количественная сторона химической реакции.
Атомно-молекулярное учение в химии
Атомно-молекулярное учение в химии окончательно утвердилось в середине XIX в. На международном съезде химиков г. Карлсруэ в 1860 г. были приняты определения понятий молекулы и атома.
Молекула – это наименьшая частица данного вещества, способная существовать самостоятельно и обладающая его химическими свойствами. Химические свойства молекулы определяются ее составом и химическим строением.
Атом – мельчайшая химически неделимая электронейтральная частица, состоящая из положительно заряженного ядра и отрицательно заряженных электронов. Атомы находятся в природе в различных формах: входят в состав простых и сложных веществ, существуют в виде ионов или одиночных атомов.
Химические элементы
Химическим элементом называется каждый отдельный вид атомов. Важнейшей характеристикой атома является положительный заряд его ядра. Таким образом, химический элемент – это определенный вид атомов с одинаковым положительным зарядом ядра.
Простые и сложные вещества. Аллотропия
Простые вещества – это вещества, образованные из атомов одного элемента.
Простое вещество отличается от понятия "химический элемент" тем, что простое вещество имеет определенный химический состав, строение, физические и химические свойства.
Пример. Простое вещества железо образовано атомами элемента железа, простое вещество азот – атомами элемента азота. Молекулы простых веществ могут состоять из одного (He, Ne), двух (О2, N2, Н2) и большего числа атомов (О3 – озон) одного элемента.
Многие химические элементы образуют несколько простых веществ, различных по строению и свойствам. Это явление называется аллотропией, а образующиеся вещества – аллотропными видоизменениями или модификациями.
Пример. Элемент кислород образует две аллотропные модификации – кислород О2 и озон О3; элемент углерод – три: алмаз, графит и карбин.
Явление аллотропии вызывается двумя причинами:
1. Различным числом атомов в молекуле (например, кислород О2 и озон О3);
2. Образованием различных кристаллических форм (например – алмаз, графит, карбин).
Сложные вещества, или химические соединения – это вещества, образованные атомами разных элементов, т.е. это устойчивая совокупность частиц (атомов, молекул, ионов), обладающая определенным составом, физическими и химическими.
Пример. Поваренная соль (NaCl) образована атомами элементов натрия и хлора, вода (Н2О) – атомами элементов водорода и кислорода.
Относительная атомная масса
Относительная атомная масса элементов – физическая величина, которая показывает, во сколько раз средняя масса атомов данного химического элемента больше 1/12 части массы атома углерода-12.
Относительные атомные массы (сложившийся термин – атомная масса) обозначается как Аr, где индекс r – начальная буква английского слова – relative – относительный.
Относительная молекулярная масса
Относительная молекулярная (формульная) масса – физическая величина, равная отношению средней массы структурной единицы данного химического вещества к 1/12 части массы атома углерода-12.
Относительная молекулярная масса показывает, во сколько раз масса молекулы данного вещества больше 1/12 массы углерода-12.
Моль. Молярная масса
Моль – это количество вещества, пропорциональное числу элементарных структурных единиц, составляющих данную порцию вещества. Зная массу одного атома углерода 1,993·10–26 кг, можно вычислить число атомов (NA) в 0,012 кг углерода:
NA = 0,012 кг / 1,993·10–26 кг = 6,02·1023
Величина NA называется постоянной Авогадро.
Химические уравнения записывают с помощью химических формул и знаков. Они служат для изображения химических реакций и отражают закон сохранения массы веществ.
В каждом уравнении имеется две части, соединенных знаком равенства. В левой части записывают формулы веществ, вступающих в реакцию, в правой – формулы веществ, образующихся в результате реакции. Число атомов каждого элемента в левой и правой частях уравнения должно быть одинаковым.
Пример:
2 Са + О2 = 2СаО.
Основные законы химии
1. Закон сохранения массы вещества – масса веществ, вступающих в химическую реакцию, равна массе веществ, образующихся в результате реакции.
Пример. При взаимодействии двух атомов молекул водорода и хлора образуется две молекулы хлористого водорода:
Н2 + Cl2 = 2HCl
Поскольку атомы имеют постоянную массу, не меняется и масса веществ до и после реакции.
2. Закон постоянства состава – всякое чистое вещество независимо от способа его получения всегда имеет постоянный качественный и количественный состав.
Пример. Углекислый газ можно получить различными способами:
– из углерода и кислорода:
С + О2 = СО2;
– из оксида углерода и кислорода:
2 СО + О2 = 2СО2;
– действием кислот на карбонаты:
СаСО3 + 2HCl = СО2 + CaCl2 + H2O и др.
Независимо от способа получения, во всех случаях чистый оксид углерода будет иметь приведенный выше состав.
3. Газовые законы. Закон Авогадро. Молекулярный объем газа.
Закон объемных отношений – объемы вступающих в реакцию газов при одинаковых условиях (температуре и давлении) относятся друг к другу как простые целые числа.
Пример. 1 л хлора соединяется с 1 л водорода, образуя 2 л хлористого водорода:
Н2 + Cl2 = 2HCl,
или 2 л оксида серы (IV) соединяются с 1 л кислорода, образуя 2 л оксида серы (VI):
2 SO2 + O2 = 2SO3.
Закон Авогадро – в равных объемах различных газов при одинаковых условиях (температура и давление) содержится одинаковое число молекул, т.е. 1 моль любого газа занимает одинаковый объем – 22,4 л/моль.
Пример расчета. При нормальных условиях, т.е. температуре 273 К и давлении 101 325 Па, масса 1 л водорода равна 0,09 г.
Молекулярная масса его равна
1,008×2 = 2,016 г/моль,
тогда объем, занимаемый 1 моль водорода, равен
2,016 г/моль:0,09 г/л = 22,4 л/моль.
При тех же условиях, масса 1 л кислорода равна 1,429 г, а его молекулярная масса – 32 г/моль, тогда объем газа равен
32 г/моль:1,429 г/л = 22,4 л/моль.
Следовательно, при нормальных условиях 1 моль различных газов занимает объем, равный 22,4 л. Этот объем называется молярным объемом газа.
Молярный объем газа – это отношение объема газа при данных условиях к количеству вещества этого газа:
VM = V(В)/n(В),
где VM и V(В) – соответственно молярный объем и объем газа В при данных условиях; n(В) – количества вещества газа В.
Строение атома
Атом состоит из положительно заряженного ядра и вращающихся вокруг ядра электронов. Атом электронейтрален, поэтому суммарный заряд электронов равен Состав атомных ядер
Ядра атомов состоят из протонов и нейтронов. Массы протона (1,673×10–27кг) и нейтрона (1,675×10–27кг) практически равны и равны примерно одной атомной единице массы (1,66×10–27). Протон обладает зарядом +1, заряд нейтрона равен 0 – частица электронейтральна.
Число протонов в атоме носит название протонного числа. Оно равно атомному номеру элемента. Атомный номер элемента называют также порядковым номером, говоря о месте элемента в периодической системе. Сумма чисел протонов (Z) и нейтронов (N) соответствуют массовому числу (А). Эти параметры связаны между собой соотношениями:
А=Z+N; Z=A-N; N=A-Z.
Пример:
2311Na 23–11=12 нейтронов;
3919K 39–19=20 нейтронов.
Атом с определенным значением атомного номера (протонного числа) и массового числа (нуклонного числа) называется нуклидом. Нуклиды с одинаковым зарядом ядра, но различными массовыми числами (А), т.е. числом нейтронов, называются изотопами (3517Cl и 3717Cl; 168O и 178О).
Состояние электрона в атоме
Большинство свойств атома определяются его электронным строением. Согласно квантово-механическим представлениям, движущемуся электрону присуща двойственная природа – дуализм. Электрон – это частица, которая имеет определённую массу и заряд. Его движение вокруг ядра носит волновой характер. Состояние электрона в атоме описывается с помощью квантово-механической модели – электронного облака. Электронная плотность облака неравномерна. По мере удаления от ядра электронная плотность возрастает и достигает максимального значения на расстоянии 0,053 нанометров (нм).
Электроны в атоме находятся лишь в определенных квантовых состояниях, соответствующих определенным значениям его энергии связи с ядром.
Значение энергии электрона является главным квантовым числом, которое может принимать только целостные значения n = 1,2,3 ….∞.
Пространство вокруг ядра, в котором наиболее вероятно нахождение электрона, называется атомной электронной орбиталью, или просто орбиталью. В зависимости от энергии электронов, орбитали имеют различные формы и размеры. Орбиталь, имеющая сферическую форму, обозначается буквой s, а электроны, образующие эту орбиталь, называются s-электронами.
Орбитали, имеющие форму объемной восьмерки (гантелей) называются р-орбиталями, а электроны, которые на них размещаются – р-электронами. Существуют d- и f-орбитали, которые имеют сложную форму, им соответствуют d- и f-электроны. На одной орбитали может находиться не более двух электронов, имеющих противоположный момент вращения вокруг оси (спин1). В этом случае два электрона называются спаренными.
Электроны с близкими значениями энергии составляют в атоме электронный слой, или энергетический уровень. Число энергетических уровней в атоме соответствует номеру периода, в котором находится химический элемент в периодической системе.
Каждый энергетический уровень обозначается своим номером: n = 1, 2, 3, 4 и т.д. или K, L, M, N, O, P, Q.
Наибольшее число электронов на энергетическом уровне равно удвоенному квадрату номера уровня:
N = 2n2
где N – число электронов;
n – номер уровня.
Значения энергии электронов одного и того же энергетического уровня могут несколько различаться, образуя подуровни (подслои). Они обозначаются буквами s, p, d, f.
Число энергетических подуровней на любом конкретном энергетическом уровне равно его номеру.
Электронное состояние атомов элементов 1–4 периодов показано в таблице
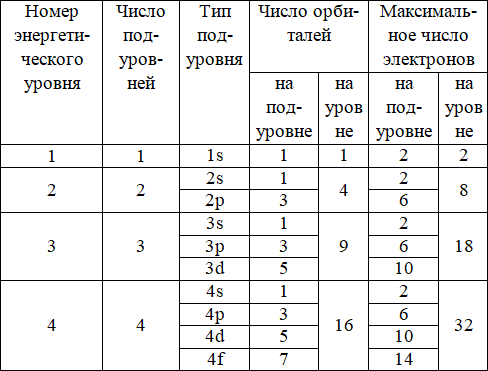
Строение электронных оболочек атомов
(Электронная структура атома)
Электроны, кроме движения вокруг ядра, обладают еще и внутренним движением, которое можно упрощенно представить как вращение вокруг собственной оси. Это явление получило название «спин» (от англ. Spin – волчок).
Электронные облака одинаковой формы могут перекрываться, если электроны обладают противоположными спинами, т.е. один как бы вращается вокруг оси по часовой стрелке, а другой против часовой стрелки ↑↓.
Энергетические уровни (слои) подразделяются на подуровни (подслои), отличающиеся друг от друга энергией связи с ядром. Число подуровней в слое зависит от его номера.
Первый энергетический уровень имеет один подуровень, второй – два, третий – три и т.д.
Подуровни в свою очередь состоят из орбиталей и соответственно называются s p d f.
Электронные формулы
Распределение электронов в атоме по энергетическим уровням изображают в виде электронных формул.
Положение электронов в атоме принято обозначать так:
– сначала цифрой указывается номер слоя;
– затем буквой подуровень;
– сверху справа от буквы число электронов на данном подуровне.
Для правильного изображения электронных конфигураций атомов необходимо соблюдать следующие правила:
– каждый электрон занимает свободную орбиталь с наиболее низкой энергией (принцип минимума энергии);
– с увеличением порядкового номера элемента электроны заполняют орбитали и уровни в порядке возрастания их энергий
– на каждой орбитали максимально может находиться не более двух электронов, причем с противоположными спинами.
Электроны располагаются на орбиталях и уровнях в порядке возрастания их энергий: уровни заполняются от первого к седьмому, а подуровни – в последовательности s-p-d-f. Последовательность возрастания энергии называется шкалой энергии.
Последовательность заполнения электронами орбиталей можно представить следующим рядом:
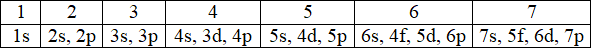
Примеры электронных формул:
1Н 1s1;
3Li 1s22s1;
6C 1s22s22p2;
7N 1s22s22p3;
9F 1s22s22p5;
10Ne 1s22s22p6;
11Na 1s22s22p63s1;
13Al 1s22s22p63s23p1;
15P 1s22s22p63s23p3;
17Cl 1s22s22p63s23p5;
19K 1s22s22p63s23p64s1.
Орбиталь с минимальной энергией – это s-орбиталь. У атома водорода она занята его единственным электроном.
На одной орбитали могут находиться два электрона, поэтому оба электрона атома гелия размещаются на 1s-орбитали. Электронная оболочка завершена и очень устойчива – это благородный газ.
У элементов второго периода заполняется L-уровень (n = 2), причем сначала орбиталь s-подуровня, а затем три орбитали р-подуровня. Третий электрон в атоме 3Li занимает 2s-орбиталь. Электрон 2s1 намного слабее связан с ядром атома, чем 1s-электроны, поэтому атом лития может его свободно терять, образуя ион лития Li+.
Далее у атомов C, N, F идет заполнение 2р-орбиталей, которое заканчивается у атома Ne.
Начиная с элементов третьего периода у атомов идет заполнение третьего M-уровня (n = 3), состоящего из 3s-, 3p-, 3d-подуровней.
Порядок заполнения электронами энергетических уровней и подуровней теоретически обосновывает периодическую систему элементов Д. И. Менделеева.
Теоретическое обоснование периодического закона
Современная формулировка периодического закона следующая:
свойства атомов химических элементов, а также состав и свойства образуемых ими веществ находятся в периодической зависимости от зарядов атомных ядер.
Сущность закона в свете современных представлений о строении атома
Период представляет собой последовательный ряд элементов, заряд ядер которых возрастает каждый раз на единицу. Очередной период начинается щелочным элементом (s-элементом) и заканчивается инертным (благородным) газом (р-элементом) с завершенной конфигурацией р-уровня.
В периодах с увеличением заряда ядра металлические свойства убывают и нарастают неметаллические свойства.
Первый период содержит два элемента: водород и гелий, у них заполняется первый электронный слой: 1Н 1s1, 2Не 1s2.
Во 2 периоде 8 элементов, и заполняется второй электронный слой:
6С 1s2222p2; 8O 1s22s22p4; 10Ne 1s22s22p5; 9F 1s22s22p5.
Третий период начинается с натрия (Na), электроны заполняют третий энергетический уровень: 11Na1s22s22p63s1. Завершается его заполнение у инертного газа аргона: 18Ar 1s22s22p63s23p6.
Четвертый период начинается калием (19К 1s22s22p63s23p64s1), его 19-й электрон занял 4s-подуровень, энергия которого ниже энергии 4d-подуровня.
В конце периода находится элемент, у которого внешний электронный слой атома заполнен. Его конфигурация включает восемь электронов.
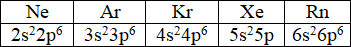
Таким образом, с увеличением заряда ядра наблюдается периодическая повторяемость электронных конфигураций внешнего слоя атомов s- и р-элементов.
Малые периоды отличаются от больших прежде всего числом элементов, а значит и их строением. Разное число элементов в периодах объясняется закономерностью заполнения электронных оболочек атомов.
Первые три периода малые (1–2 электрона, 2 и 3–8 электронов).
В 4-ом периоде 18 элементов, два первых – это s-элементы (К, Са), в атомах которых заполняется внешний электронный слой (4 s-орбиталь). Последние 6 элементов – это р-элементы. В их атомах заполняется внешний слой (4р-орбиталь). Между s- и р-элементами расположены 10 d-элементов. В их атомах заполняются d-орбитали предвнешнего электронного слоя.
Подобная же картина наблюдается в 5-ом периоде, состоящем из 18 элементов. В нем также 2 s-элемента, 10 d-элементов и 6 р-элементов.
Шестой период состоит из 32 элементов. Это 2 s-элемента, 10 d-элементов, 6 р-элементов и 14 f-элементов, которые вынесены за пределы таблицы.
Седьмой период незавершенный. Заполнение электронами электронных уровней аналогично 6-ому периоду. После заполнения 7s-подуровня у франция (Z=87) и радия (Z=88) электрон актиния поступает на 6d-подуровень, после которого начинается заполнение 5f-подуровня 14 электронами. Это происходит у атомов элементов актиноидов с Z=90…103. После 103-го элемента идет заполнение 6d-подуровня: у резерфордия (Z=104), дубния (Z=105), сиборгия (Z=106), бория (Z=107) и т.д. Актиноиды, как и лантоноиды, обладают многими сходными химическими свойствами.
От всех других групп отличается VIII группа. Помимо главной подгруппы имеется побочная подгруппа, состоящая и из 9 элементов: семейство железа (Fe, Co, Ni) и семейство платины (Ru, Rh, Pb, Os, Ir, Pt).
В главную подгруппу входят s- и р-элементы, а в побочную d-элементы.
Таким образом, структура периодической системы связана с электронной структурой элементов. В периодической системе все химические элементы располагаются в порядке возрастания атомных номеров элементов. Величина атомного номера соответствует положительному заряду ядра атома соответствующего элемента. В периодической системе 7 периодов и 18 групп (8 групп А и 10 групп В). С увеличением зарядов ядер происходит постепенное заполнение электронных структур атомов в соответствии с принципами заполнения. Следовательно, структура периодической системы связана с электронной структурой элементов.
В зависимости от того, какой энергетический подуровень заполняется электронами последним, различают четыре типа элементов:
1) s-элементы (завершается s-подуровень),
2) р-элементы (заполняется р-подуровень),
3) d-элементы (заполняется d-подуровень предвнешнего энергетического уровня) и
4) f-элементы (заполняется предпредвнешний энергетический уровень, f-подуровень).
Номер периода указывает на число энергетических уровней, на которых находятся электроны в атомах конкретного элемента, и именно в этом заключается физический смысл номера периода. В периоде с увеличением заряда ядра атомов наблюдается постепенное изменение свойств от металлических к неметаллическим. Такое изменение свойств объясняется увеличением числа электронов на внешнем энергетическом уровне атомов. Первые три периода содержат только s- и р-элементы, последующие три включают в свой состав также также d-и f-элементы, которые образуют В-группы (побочные).
В группах объединены элементы, которые имеют сходное электронное строение внешнего энергетического уровня.
Номер группы, в которой находится элемент, указывает на максимальное число электронов, которое может участвовать в образовании химических связей, т.е. валентных электронов. В этом состоит физический смысл номера группы.
Связь периодической системы элементов с теорией строения атомов
1. Порядковый номер элемента соответствует значению заряда ядра (количество протонов) и числу электронов на энергетических уровнях в его атоме.
Возрастание положительных зарядов атомных ядер от 1 до 107 приводит к периодическому повторению строения электронных оболочек атомов, от чего зависят химические свойства элементов.
2. Номер периода соответствует числу энергетических уровней в атомах данного элемента.
3. Периодичность изменения химических свойств элементов зависит от периодичности расположения электронов по энергетическим уровням.
4. Возрастание высших степеней окисления в соединениях с кислородом и уменьшение степеней окисления в соединениях с водородом в периодах слева направо объясняется увеличением числа электронов на внешних энергетических уровнях.
5. В периодах слева направо заряд ядра постепенно увеличивается, и расстояние между ядром и внешними электронами сокращается. В связи с этим отдача электронов постепенно затрудняется, и металлические свойства ослабевают.
В больших периодах с ростом заряда ядер заполнение электронов происходит сложнее – в четных рядах с ростом положительного заряда ядра число электронов во внешнем уровне остается постоянным и равно 2, редко 1, идет заполнение предпоследнего уровня, и свойства элементов изменяются очень медленно.
6. Номер группы указывает на число электронов, которые могут участвовать в образовании химической связи. Высшая степень окисления с кислородом соответствует числу электронов, находящихся на внешнем энергетическом уровне (число валентных электронов соответствует номеру группы). Baлентность в соединении с водородом определяется числом электронов, недостающих до числа 8.
Деление на подгруппы основано на различии в заполнении электронами энергетических уровней.
У элементов главных подгрупп заполняются или s-подуровни, или р-подуровни внешних уровней.
У элементов побочных подгрупп заполняются d-подуровни второго снаружи уровня.
В каждой подгруппе объединены элементы, атомы которых имеют сходное строение внешнего электронного уровня.

